Evaluarea Hormonala la Femei: Ghid Complet pentru Sănătatea Endocrinologică și Ginecologică
- Dr. Allia Dmour

- May 2
- 14 min read

Articol: Evaluarea Hormonala la Femei: Ghid Complet pentru Sănătatea Endocrinologică și Ginecologică
Autor:
Dr. Elena Ciobanu
Medic specialist Endocrinologie
-Echipa medicală a Clinicii Doctor Allia Dmour, Iași-
Categorie: Endocrinologie | Ginecologie | Esențiale pentru Sănătatea Femeii
Timp estimat de lectură: 12 minute
Publicat: 2026 | Actualizat continuu conform ghidurilor internaționale
Dezechilibrele hormonale reprezintă una dintre cele mai frecvente cauze ale consultației medicale în ginecologie și endocrinologie la femei. De la perioada de adolescență târzie până la perimenopauză și postmenopauză, sistemul endocrin feminin se confruntă cu numeroase provocări: cicluri menstruale neregulate, tulburări de fertilitate, afecțiuni tiroidiene autoimune, sindromul ovarelor polichistice (SOP) și modificări metabolice complexe. Evaluarea hormonală completă reprezintă fundamentul diagnostic al tuturor acestor condiții.
Prezentul articol oferă un ghid clinic și educațional aprofundat despre profilul hormonal al femeii, incluzând tiroida, hormonii sexuali, androgenii, cortizolul, rezerva ovariană și indicatorii metabolici. Informațiile sunt bazate pe cele mai recente ghiduri internaționale (Endocrine Society, ESHRE, ACOG, ETA) și adaptate contextului clinic integrat ginecologie-endocrinologie practicat în cadrul Clinicii Doctor Allia Dmour din Iași.
1. De ce este importantă evaluarea hormonală la femei?
Hormonii sunt mesagerii chimici care reglează practic fiecare funcție fiziologică: metabolismul, reproducerea, dispoziția, somnul, greutatea corporală, sănătatea osoasă și răspunsul imun. La femei, echilibrul hormonal este deosebit de complex datorită fluctuațiilor ciclice ale estrogenului și progesteronului, interacțiunii cu axa tiroidiană și suprarenaliană și impactului pe care factori externi (stres, alimentație, somn) îl exercită asupra producției hormonale.
Organizația Mondială a Sănătății (OMS) estimează că tulburările endocrine afectează sute de milioane de persoane la nivel global, femeile reprezentând grupul cu cea mai mare prevalență a afecțiunilor tiroidiene, autoimune și reproductive. Un raport Lancet din 2019 subliniază că hipotiroidismul netratat la femei de vârstă fertilă crește semnificativ riscul de avort spontan, de naștere prematură și de afectare a neurodezvoltării fetale, ceea ce face screeningul tiroidian o prioritate de sănătate publică.
De reținut:
|
2. Principalii hormoni evaluați la femei – Profil complet
Un profil hormonal complet la femeie cuprinde mai multe categorii de investigații, organizate pe axe endocrine distincte, dar cu puternice interacțiuni clinice:
2.1 Axa tiroidiană
Tiroida este o glandă cu rol central în metabolismul bazal, termoregulare, dezvoltarea neurologică și fertilitate. Evaluarea tiroidiană standard include:
TSH (hormonul tireostimulant) – testul de screening de primă linie. Valorile normale: 0,4–4,0 mUI/L (varianță la gravide: 0,1–2,5 mUI/L în T1).
FT4 (tiroxina liberă) – reflectă producția tiroidiană; valorile normale: 12–22 pmol/L.
FT3 (triiodotironina liberă) – forma activă metabolic; utilă în hipotiroidism subclinic și monitorizarea tratamentului cu levotiroxină.
Anti-TPO (anticorpi anti-tireoperoxidază) – marker principal al autoimunității tiroidiene; pozitivitate în tiroidita Hashimoto și boala Graves.
Anti-TG (anticorpi anti-tireoglobulină) – complementar anti-TPO; importanți în caz de Anti-TPO negativ cu suspiciune clinică.
Ecografia tiroidiană – nu este un test hormonal, dar completează evaluarea în caz de noduli, volumetrie tiroidiană sau pattern ecografic sugestiv pentru autoimunitate.
Conform Ghidului American Thyroid Association (ATA, 2019) și European Thyroid Association (ETA, 2021), screeningul tiroidian este recomandat în mod special la: femeile ce planifică o sarcină, în primele 8–10 săptămâni de sarcină, la femeile cu istoric familial de afecțiune tiroidiană și la toate femeile simptomatice (oboseală, modificări de greutate, frilozitate, palpitații).
2.2 Hormonii sexuali și axa gonadotropă
FSH (hormonul foliculo-stimulant) – reglează maturarea foliculară; valori crescute sugerează rezervă ovariană scăzută sau menopauză (> 40 UI/L postmenopauză).
LH (hormonul luteinizant) – declanșează ovulația; raportul LH/FSH > 2 este sugestiv pentru SOP.
Estradiol (E2) – principalul estrogen feminin; valori scăzute în menopauză, insuficiență ovariană prematură; valori crescute în chisturi foliculare, tumori estrogenice.
Progesteron – dozat în ziua 21 a ciclului (faza luteală); valori > 3 ng/mL confirmă ovulația.
AMH (hormonul anti-Müllerian) – cel mai precis marker al rezervei ovariene; se poate doza în orice zi a ciclului menstrual; valori scăzute = rezervă ovariană diminuată; valori crescute = SOP.
2.3 Androgenii
Testosteron total și liber – evaluat în hiperandrogenism (acnee, hirsutism, alopecie); crescut în SOP, hiperplazie suprarenaliană congenitală.
DHEA-S (sulfat de dehidroepiandrosteron) – androgen suprarenalian; util în diferențierea sursei de hiperandrogenism (ovariană vs. suprarenaliană).
17-OH progesteron – screening pentru hiperplazia suprarenaliană congenitală cu deficit de 21-hidroxilază.
SHBG (globulina de legare a hormonilor sexuali) – scăzută în rezistența la insulină și SOP; afectează biodisponibilitatea testosteronului.
2.4 Prolactina
Prolactina este secretată de hipofiza anterioară și are rol principal în lactație. Hiperprolactinemia (valori crescute ale prolactinei) este o cauză frecventă de amenoree, galactoree, infertilitate și tulburări de libidou. Cauzele includ prolactinomul hipofizar (adenom benign), hipotiroidismul primar, medicamentele (antipsihotice, antiemetice) și stresul acut. Evaluarea prolactinei se face dimineața, à jeun, în repaus, evitând stimulii mecanici în ziua recoltării.
2.5 Cortizolul și axa hipotalamo-hipofizo-suprarenaliană (HHS)
Cortizolul este hormonul principal al răspunsului la stres, secretat de cortexul suprarenal sub controlul ACTH. Valorile normale dimineața (8:00): 6,2–19,4 μg/dL. Hipercortizolemie (sindrom Cushing) – asociat cu obezitate abdominală, hirsutism, diabet; hipocortizolism (boala Addison) – oboseală severă, hipotensiune, hiperpigmentare. Dozarea cortizolului este esențială în evaluarea obezității refractare la femei și în suspiciunea de disfuncție suprarenaliană.
2.6 Insulina, glicemia și indexul HOMA-IR
Rezistența la insulină este un numitor comun în SOP, obezitate, sindrom metabolic și NAFLD (boală hepatică grasă non-alcoolică). Evaluarea include: glicemie à jeun, insulina à jeun și calculul HOMA-IR = (insulina à jeun [μUI/mL] × glicemia à jeun [mmol/L]) / 22,5. Un HOMA-IR > 2 semnifică rezistență la insulină. Conform unui studiu publicat în Journal of Clinical Endocrinology & Metabolism (2020), > 70% din femeile cu SOP prezintă rezistență la insulină, indiferent de indicele de masă corporală.
3. Tabel de referință – Profile hormonale la femei
Tabelul de mai jos sintetizează principalii parametri hormonali, valorile normale orientative și semnificația lor clinică. Valorile de referință pot varia ușor în funcție de laboratorul utilizat, metoda de dozare și faza ciclului menstrual:
Hormon / Test | Valori normale orientative | Semnificație clinică |
TSH (tireotrof) | 0,4 – 4,0 mUI/L | Screening tiroidian de primă linie |
FT4 (tiroxina liberă) | 12 – 22 pmol/L | Funcția tiroidiană secretorie |
FT3 (triiodotironina liberă) | 3,1 – 6,8 pmol/L | Forma activă a hormonului tiroidian |
Anti-TPO (anticorpi anti-tireoperoxidază) | < 35 UI/mL | Autoimunitate tiroidiană (Hashimoto, Graves) |
Anti-TG (anticorpi anti-tireoglobulină) | < 115 UI/mL | Tiroidită autoimună |
FSH (foliculo-stimulant) | 3,5 – 12,5 UI/L (faza foliculară) | Rezervă ovariană, menopauză |
LH (luteinizant) | 2,4 – 12,6 UI/L (faza foliculară) | Ovulație, SOP |
Estradiol (E2) | 30 – 400 pg/mL (ciclu) | Sănătate reproductivă, menopauză |
Progesteron | 1 – 28 ng/mL (faza luteală) | Confirmarea ovulației, corp lutein |
Testosteron total | 0,06 – 0,82 ng/mL (femei) | Hiperandrogenism, SOP, libidou |
DHEA-S (sulfat de dehidroepiandrosteron) | 35 – 430 μg/dL | Androgeni suprarenalieni |
Prolactina | 4,8 – 23,3 ng/mL | Galactoree, tulburări de ciclu, adenoame |
AMH (hormon anti-Müllerian) | 1,0 – 3,5 ng/mL (25–35 ani) | Rezerva ovariană; fertilitate |
Cortizol (dimineața, 8:00) | 6,2 – 19,4 μg/dL | Axul hipotalamo-hipofizo-suprarenal |
Insulina à jeun | 2 – 25 μUI/mL | Rezistență la insulină (HOMA-IR) |
HOMA-IR | < 2,5 | Index de rezistență insulinică |
Surse: Endocrine Society Clinical Practice Guidelines (2023); ATA Guidelines (2019); ETA Guidelines (2021); ESHRE Guidelines on PCOS (2023); LabCorp & Mayo Clinic Reference Ranges (2024).
4. Evaluarea tiroidiană la femei – o prioritate clinică în ginecologie-endocrinologie
Afecțiunile tiroidiene sunt cu diferență cele mai frecvente boli endocrine la femei, cu o prevalență estimată de 5–10% pentru hipotiroidismul manifest și 10–15% pentru tiroidita Hashimoto în populația generală feminină (Vanderpump, Lancet Diabetes & Endocrinology, 2011). Această realitate epidemiologică impune ca evaluarea tiroidiană să fie parte integrantă a oricărui consult ginecologic de rutină, nu doar al celui endocrinologic.
4.1 Tiroidita Hashimoto – cea mai frecventă cauză de hipotiroidism la femei
Tiroidita Hashimoto este o afecțiune autoimună în care sistemul imunitar produce anticorpi împotriva tireoperoxidazei (Anti-TPO) și tireoglobulinei (Anti-TG), ducând la distrugerea progresivă a parenchimului tiroidian. Prevalența este de 5–10% la femeile de vârstă reproductivă și crește după vârsta de 40 de ani. Simptomele includ oboseală cronică, creștere în greutate, depresie, constipație, frilozitate și tulburări de ciclu menstrual. Conform unei meta-analize publicată în Thyroid (2019), Anti-TPO pozitiv a fost asociat cu un risc de 3,7 ori mai mare de avort spontan, independent de funcția tiroidiană.
4.2 Hipotiroidismul subclinic și fertilitatea
Hipotiroidismul subclinic (TSH crescut cu FT4 normal) este un domeniu controversat, dar studii recente sugerează că femeile cu TSH > 2,5 mUI/L și Anti-TPO pozitiv prezintă rate mai scăzute de implantare în procedurile de reproducere asistată și un risc mai mare de complicații obstetricale. Ghidul ETA (2021) recomandă tratamentul cu levotiroxină la femeile cu TSH > 2,5 mUI/L ce planifică o sarcină sau urmează tratamente de fertilitate.
4.3 Boala Graves și hipertiroidismul
Boala Graves este principala cauză de hipertiroidism la femei (80–85% din cazuri), mediată de anticorpi stimulatori ai receptorului TSH (TRAb). Se manifestă prin palpitații, tremor, pierdere în greutate, intoleranță la căldură, exoftalmie și, la femei, tulburări de ciclu menstrual. Tratamentul implică antitiroidiene de sinteză, radioiod sau tiroidectomie, cu monitorizare atentă în sarcină, întrucât TRAb traversează placenta și poate cauza hipertiroidism neonatal (ACOG, 2020).
5. Tulburări hormonale frecvente la femei – prezentare clinică
5.1 Sindromul ovarelor polichistice (SOP)
SOP este cea mai frecventă afecțiune endocrină la femeile de vârstă reproductivă, afectând 8–13% din această populație (ESHRE/ASRM, 2023). Diagnosticul se bazează pe criteriile Rotterdam (2003): oligo/anovulație, hiperandrogenism clinic sau biochimic și aspect ecografic de ovare polichistice, cu excluderea altor cauze. Profilul hormonal tipic include: LH crescut, uneori raport LH/FSH > 2, testosteron crescut, AMH crescut (deseori > 5 ng/mL), rezistență la insulină și, frecvent, TSH la limita superioară.
Conform celui mai recent Ghid Internațional ESHRE 2023 privind SOP, evaluarea optimă include: FSH, LH, estradiol, testosteron total, DHEA-S, AMH, TSH, HOMA-IR și prolactina (pentru excluderea hiperprolactinemiei). Managementul terapeutic este complex și necesită abordare interdisciplinară ginecologie-endocrinologie.
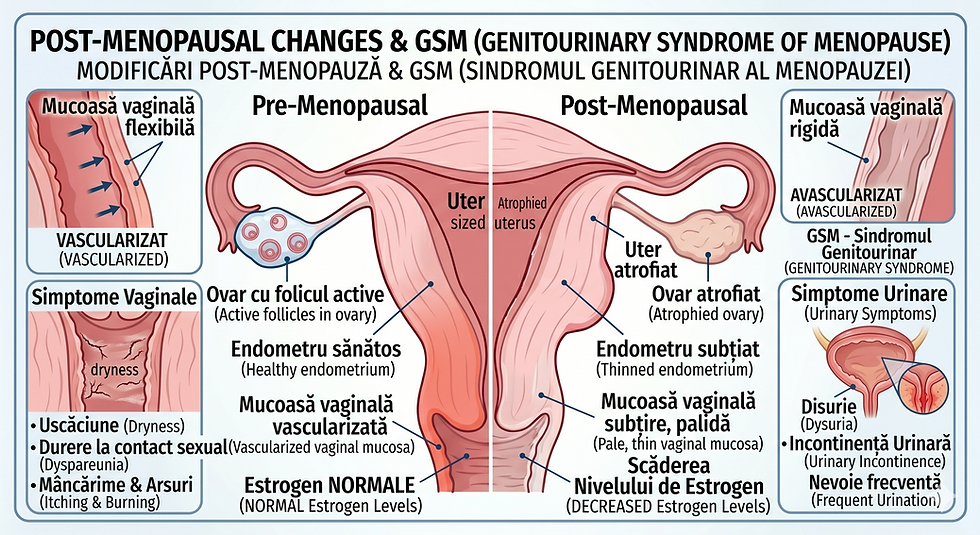
5.2 Perimenopauza și menopauza
Tranziția menopauza este asociată cu declinul producției de estrogeni și progesteron ovarian, cu creșterea compensatorie a FSH și LH. Menopauza este confirmată clinic după 12 luni de amenoree și biochimic prin FSH > 25 UI/L și estradiol < 20 pg/mL. Simptomele climacterice (bufeuri, transpirații nocturne, tulburări de somn, simptome genitourinare, modificări cognitive) afectează 75–80% din femei (Menopause Society, 2023). Evaluarea hormonală în perimenopauza ghidează decizia de inițiere a terapiei hormonale menopauza (THM), personalizate în funcție de riscuri și beneficii individuale.
5.3 Insuficiența ovariană prematură (IOP)
IOP (numită și insuficiență ovariană primară) este definită ca instalarea menopauzei înainte de vârsta de 40 de ani, afectând aproximativ 1–2% din femei. Diagnosticul hormonal: FSH > 25 UI/L la două recoltări separate la interval de 4–6 săptămâni, asociat cu estradiol scăzut și oligo/amenoree. IOP poate fi autoimună (uneori asociată cu tiroidita Hashimoto), iatrogenă (chimioterapie, radioterapie), genetică (sindrom Turner, premutație FMR1) sau idiopatică. Impactul este major asupra fertilității, densității osoase și sănătății cardiovasculare pe termen lung.
5.4 Hiperandrogenismul feminin
Excesul de androgeni la femei se manifestă prin: hirsutism (scoring Ferriman-Gallwey ≥ 8), acnee persistentă la femei adulte, alopecie androgenetică și virilizare (în cazuri severe). Cauzele principale sunt SOP (> 70% din cazuri), hiperplazia suprarenaliană congenitală (HCS) cu deficit de 21-hidroxilază (forma tardivă), tumorile secretante de androgeni și sindromul Cushing. Profilul hormonal include: testosteron total și liber, DHEA-S, 17-OH progesteron (recoltare dimineața în faza foliculară precoce), cortizol și TSH.
6. Când este indicat un profil hormonal complet? – Ghid practic
Evaluarea hormonală este indicată în mai multe contexte clinice. Tabelul de mai jos prezintă principalele motive de prezentare și investigațiile hormonale corespunzătoare, conform recomandărilor Endocrine Society, ESHRE și ACOG:
Motiv de prezentare / simptom | Investigații hormonale recomandate |
Tulburări de ciclu menstrual (oligomenoree, amenoree) | FSH, LH, estradiol, progesteron, prolactina, TSH, testosteron, DHEAS, cortizol, AMH |
Suspiciune hipotiroidism / hipertiroidism | TSH, FT4, FT3, Anti-TPO, Anti-TG, TRAb |
Sindromul ovarelor polichistice (SOP) | FSH, LH, raport LH/FSH, estradiol, testosteron, DHEA-S, androstendion, 17-OH-Progesteron, prolactina, HOMA-IR, AMH, TSH |
Infertilitate / planificare sarcină | AMH, FSH, LH, estradiol, progesteron, testosteron, DHEAS, cortizol, TSH, prolactina, Anti-TPO, AAT-TG |
Perimenopauză / menopauză | FSH, LH, estradiol, TSH, cortizol |
Hirsutism / alopecie androgenetică | LH, FSH, estradiol, Testosteron total/liber, DHEA-S, 17-OH progesteron, androstendion, cortisol, TSH, ATPO, AAT-TG. |
Acnee severă la femei adulte | LH, FSH, estradiol, Testosteron, DHEA-S, prolactină, cortizol, TSH, HOMA-IR |
Oboseală cronică, creștere în greutate inexplicabilă | TSH, FT4, cortizol, HOMA-IR, prolactină, LH, FSH, Testosteron, estradiol, DHEAS |
Osteoporoză prematură | FSH, estradiol, TSH, PTH, 25-OH-vitamina D |
Screening preventiv (> 35 de ani) | TSH, FSH, estradiol, AMH, prolactina, glicemie à jeun, insulina a jeun |
Nota importantă: recoltarea analizelor hormonale necesită o pregătire corectă – recoltare dimineața între orele 7:00–9:00, à jeun (minimum 8–10 ore), în repaus, evitând efortul fizic intens în ziua premergătoare și informând medicul despre orice medicație curentă (pilule contraceptive, levotiroxina, corticosteroizi) care poate influența rezultatele.
7. Cum se desfășoară evaluarea hormonală integrată la Clinica Doctor Allia Dmour
Clinica Doctor Allia Dmour din Iași oferă un model integrat ginecologie-endocrinologie, unic în Moldova, care permite evaluarea hormonală completă a femeii cu o abordare multidisciplinară coordonată. Parcursul pacientei include:
Consultații inițiale integrat – medicul endocrinolog și ginecologul evaluează împreună istoricul medical, simptomatologia, antecedentele obstetricale, familiale și heredocolaterale.
Stabilirea profilului hormonal personalizat – în funcție de tabloul clinic, se recomandă investigațiile specifice, evitând supradozarea inutilă de analize sau, dimpotrivă, omiterea unor parametri esențiali.
Recoltarea și interpretarea rezultatelor – rezultatele sunt analizate în contextul clinic complet, ținând cont de faza ciclului menstrual, vârstă, medicație și istoricul reproducției.
Planul terapeutic individualizat – poate include tratament medicamentos (levotiroxina, metformin, antiandrogene, progesteron, terapie hormonală menopauza), modificări ale stilului de viață sau trimitere pentru investigații suplimentare (ecografie tiroidiană, RMN hipofizar, densitometrie osoasă).
Monitorizarea pe termen lung – dezechilibrele hormonale sunt afecțiuni cronice ce necesită monitorizare periodică; intervalele de reevaluare sunt stabilite individualizat.
De ce ginecologie + endocrinologie în aceeași clinică medicală? Cele două specialități sunt profund interconectate la femei. Tiroidita Hashimoto influențează fertilitatea și ciclul menstrual. SOP implică atât hiperandrogenism (endocrinologie) cât și tulburări de ovulație (ginecologie). Menopauza presupune decizii terapeutice complexe (THM) care necesită expertiză în ambele domenii. Managementul dezechilibrelor hormonale este incomplet dacă cele două specialități funcționează separat. |
Despre autor:
Dr. Elena Ciobanu este medic specialist endocrinologie în cadrul Clinicii Doctor Allia Dmour din Iași, absolventă a Facultății de Medicină a Universității de Medicină și Farmacie „Gr. T. Popa" Iași. Și-a perfecționat competențele prin cursuri de supraspecializare în endocrinologie, ecografie endocrinologică și tehnică de puncție-aspirație cu ac fin a nodulilor tiroidieni.
Este absolventă a programului „Nutrition Science" de la Stanford Center for Health Education și a programului „Managementul Serviciilor de Sănătate" organizat de Institutul Național de Management al Serviciilor de Sănătate.
Cu peste 30.000 de consultații de-a lungul carierei, Dr. Elena Ciobanu s-a dedicat diagnosticării și tratării patologiilor sistemului endocrin la adulți, copii și adolescenți, obținând rezultate deosebite în afecțiunile tiroidiene și suprarenaliene, tratamentul infertilității, tulburările de creștere și pubertate, obezitate, menopauză și osteoporoză. Oferă consultații endocrinologice la nivel de expert, evaluarea hormonala la femei și ecografii Doppler tiroidiene în cadrul Clinicii Doctor Allia Dmour.
8. Întrebări frecvente (FAQ) – Evaluarea Hormonală la Femei
Q1. Ce analize hormonale sunt recomandate femeilor pentru un profil hormonal complet?
Un profil hormonal complet la femei include: TSH, FT4, FT3, anti-TPO (tiroida), FSH, LH, estradiol, progesteron, testosteron total, DHEA-S (hormoni sexuali și androgeni), prolactina, AMH (rezervă ovariană), cortizol dimineața și insulina à jeun cu calcularea HOMA-IR. Medicul endocrinolog va personaliza lista de investigații în funcție de simptome, vârstă și obiectivele clinice.
Q2. Când trebuie să îmi fac analizele hormonale în raport cu ciclul menstrual?
Majoritatea hormonilor sexuali (FSH, LH, estradiol) se recoltează în zilele 2–5 ale ciclului menstrual (faza foliculară precoce). Progesteronul se dozează în ziua 21–23 (faza luteală mijlocie) pentru confirmarea ovulației. TSH, prolactina, cortizolul și insulina pot fi recoltate oricând în ciclu, dimineața à jeun. AMH are avantajul că poate fi dozat în orice zi a ciclului, cu variabilitate redusă.
Q3. Ce simptome indică un dezechilibru hormonal la femei?
Simptomele frecvente ale dezechilibrului hormonal includ: neregularități menstruale, oboseală cronică, creștere sau scădere inexplicabilă în greutate, acnee sau hirsutism la femei adulte, căderea excesivă a părului, tulburări de somn, modificări ale dispoziției, dificultăți de concentrare, senzație de frig sau căldură excesivă, palpitații și probleme de fertilitate. Orice combinație a acestor simptome justifică o evaluare hormonală completă.
Q4. De ce este evaluarea tiroidiană atât de importantă la femei?
Femeile sunt de 5–10 ori mai predispuse decât bărbații la afecțiuni tiroidiene autoimune. Hipotiroidismul netratat afectează fertilitatea, sarcina (risc de avort spontan, naștere prematură, tulburări de neurodezvoltare fetală) și calitatea vieții generale. Screeningul tiroidian este recomandat înainte de concepție, în primul trimestru de sarcină și la femeile cu simptome sugestive. TSH este testul de primă linie, completat cu FT4, FT3 și anticorpi anti-TPO.
Q5. Care este diferența dintre un consult endocrinologic și un consult ginecologic pentru probleme hormonale?
Ginecologul evaluează în principal hormonii sexuali în relație cu sănătatea reproductivă (ciclu menstrual, ovulație, sarcină, menopauză), în timp ce endocrinologul are o perspectivă sistemică, evaluând și tiroida, suprarenalele, metabolismul glucozei și alte axe hormonale. La Clinica Allia din Iași, specialitățile sunt integrate, permițând un management interdisciplinar complet – avantaj major în condiții precum SOP, tiroidita Hashimoto asociată infertilității sau dezechilibrele hormonale din perimenopauză.
Q6. Cât de des trebuie repetate analizele hormonale?
Frecvența depinde de contextul clinic. La femeile tratate pentru hipotiroidism, TSH se verifică la 6–8 săptămâni după orice modificare de doză, apoi anual. La femeile cu SOP, monitorizarea se face semestrial sau anual. Profilul hormonal complet se recomandă anual pentru femeile peste 35 de ani sau mai frecvent dacă există simptome active. Medicul endocrinolog va stabili intervalele optime de monitorizare individual.
Q7. Poate dezechilibrul tiroidian influența greutatea corporală la femei?
Da. Hipotiroidismul reduce rata metabolismului bazal, ducând frecvent la creștere în greutate, retenție de apă, constipație și oboseală. Hipertiroidismul accelerează metabolismul și poate cauza pierdere în greutate, transpirații și palpitații. Orice modificare inexplicabilă de greutate trebuie investigată prin dozarea TSH, FT4 și FT3, deoarece tratamentul corect al afecțiunii tiroidiene normalizează în general greutatea corporală.
Q8. Ce este AMH și de ce este important în evaluarea hormonală?
AMH (hormonul anti-Müllerian) este produs de celulele granuloase ale foliculilor ovarieni și reflectă direct rezerva ovariană. Valorile scăzute indică o rezervă ovariană diminuată – relevant în planificarea fertilității și prognosticul menopauzei. Valorile crescute (> 5 ng/mL) sunt frecvente în SOP. AMH are avantajul de a putea fi dozat în orice zi a ciclului menstrual, cu variabilitate minimă, ceea ce îl face investigația de elecție pentru evaluarea rezervei ovariene.
📍 Programează-te la o consultație de endocrinologie la Clinica Doctor Allia Dmour Iași Ai simptome care te îngrijorează? Cicluri neregulate, oboseală inexplicabilă, modificări de greutate, acnee persistentă sau tulburări de fertilitate? Nu amâna evaluarea hormonală. La Clinica Doctor Allia Dmour din Iași, beneficiezi de evaluare hormonală completă într-un model integrat de ginecologie și endocrinologie. Dr. Elena Ciobanu (medic specialist endocrinologie) și Dr. Allia Dmour (medic primar obstetrică-ginecologie, doctor în medicină) colaborează pentru un diagnostic precis și un plan terapeutic personalizat. 🏥 Clinica Doctor Allia Dmour | Bd. Carol I nr. 48, Iași 📞 0747 619 919 | 0371 371 381 → Programează online | → Vezi tarife | → Endocrinologie | → Ginecologie |
⚠️Disclaimer medical
Conținutul acestui articol are caracter strict informativ și educațional. Nu constituie sfat medical, diagnostic sau recomandare terapeutică individuală. Fiecare pacient și ficare caz necesită evaluare individualizată. Consultați întotdeauna un medic specialist înainte de a începe, modifica sau întrerupe orice tratament. Valorile de referință hormonale prezentate sunt orientative și pot varia în funcție de metodologia laboratorului.
Bibliografie selectivă
Articolul a fost redactat pe baza ghidurilor internaționale cu cel mai înalt nivel de evidență și a literaturii medicale peer-reviewed:
1. Endocrine Society. Clinical Practice Guidelines: Management of Thyroid Dysfunction During Pregnancy and Postpartum. J Clin Endocrinol Metab. 2023.
2. Alexander EK, et al. 2017 Guidelines of the American Thyroid Association for the Diagnosis and Management of Thyroid Disease During Pregnancy and the Postpartum. Thyroid. 2017;27(3):315–389.
3. Jonklaas J, et al. Guidelines for the Treatment of Hypothyroidism: Prepared by the American Thyroid Association Task Force on Thyroid Hormone Replacement. Thyroid. 2014;24(12):1670–1751.
4. Thyroid ETA Working Group. 2021 European Thyroid Association Guideline for the Management of Subclinical Hypothyroidism in Pregnancy. Eur Thyroid J. 2021.
5. Teede HJ, et al. Recommendations from the 2023 International Evidence-Based Guideline for the Assessment and Management of Polycystic Ovary Syndrome. Fertil Steril. 2023;120(4):767–793. (ESHRE/ASRM)
6. Lizneva D, et al. Criteria, Prevalence, and Phenotypes of Polycystic Ovary Syndrome. Fertil Steril. 2016;106(1):6–15.
7. Vanderpump MP. The Epidemiology of Thyroid Disease. Br Med Bull. 2011;99:39–51.
8. Negro R, et al. Hypothyroidism and Pregnancy Loss. Best Pract Res Clin Endocrinol Metab. 2019;33(1):26–31. (Thyroid, meta-analysis)
9. ACOG Practice Bulletin No. 223: Thyroid Disease in Pregnancy. Obstet Gynecol. 2020;135(6):e261–e274.
10. Azziz R, et al. Polycystic Ovary Syndrome. Nat Rev Dis Primers. 2016;2:16057.
11. Dunaif A, et al. Insulin Resistance and the Polycystic Ovary Syndrome: Mechanism and Implications for Pathogenesis. Endocr Rev. 2016.
12. La Marca A, Giulini S, Tirelli A, et al. Anti-Müllerian Hormone Measurement on any Day of the Menstrual Cycle Strongly Predicts Ovarian Response in Assisted Reproductive Technology. Hum Reprod. 2007;22(3):766–771.
13. The Menopause Society (NAMS). 2023 Menopause Hormone Therapy Position Statement. Menopause. 2023;30(6):573–625.
14. Webber L, et al. ESHRE Guideline: Management of Women with Premature Ovarian Insufficiency. Hum Reprod. 2016;31(5):926–937.
15. Nieschlag E, Swerdloff R, et al. Endocrine Society. Investigation, Treatment and Monitoring of Late-onset Hypogonadism in Males. J Clin Endocrinol Metab. 2006 (adaptat pentru referință croise femei).
16. Mastorakos G, Valsamakis G, Papatheodorou D, et al. Cushing's Syndrome in Women of Reproductive Age. Best Pract Res Clin Endocrinol Metab. 2015;29(3):391–401.
17. Bianco AC, et al. American Thyroid Association Task Force on Combination T4 and T3 Therapy. Thyroid. 2019;29(10):1284–1346.
18. Zimmermann MB, Boelaert K. Iodine Deficiency and Thyroid Disorders. Lancet Diabetes Endocrinol. 2015;3(4):286–295.
19. The Lancet Diabetes & Endocrinology. Thyroid Function, Pregnancy Loss, and Fertility. Lancet Diabetes Endocrinol. 2019;7(7):503–504.
20. Pasquali R, et al. Insulin and the Polycystic Ovary Syndrome. J Clin Endocrinol Metab. 2020;105(9):e3070–e3079.



Comments