Sindromul Ovarelor Polichistice (SOP): cauze, simptome, diagnostic, fertilitate și soluții integrate
- Dr. Allia Dmour

- 4 days ago
- 16 min read
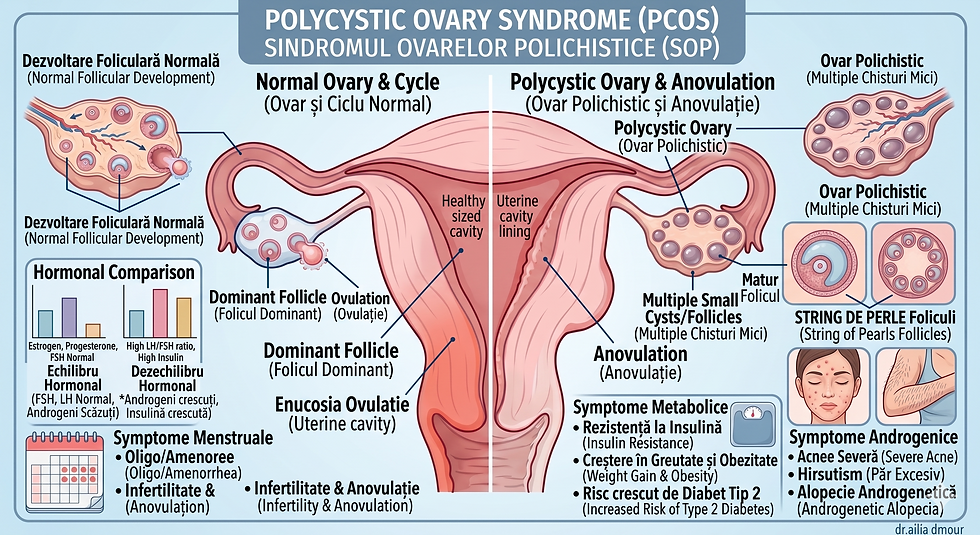
Articol: Sindromul Ovarelor Polichistice (SOP), cauze, simptome, diagnostic, fertilitate și soluții integrate
Autor: Dr. Allia Dmour | Medic primar obstetrică-ginecologie, Doctor în Științe Medicale
Categorie: Esențiale pentru Sănătatea Femeii | Ginecologie | Endocrinologie
Timp estimat de lectură: 9 minute
Introducere: SOP — cea mai frecventă tulburare hormonală la femeia de vârstă fertilă
Sindromul Ovarelor Polichistice — abreviat SOP (în engleză, PCOS — Polycystic Ovary Syndrome) — este cea mai frecventă tulburare endocrino-metabolică a femeilor de vârstă reproductivă. Afectează între 8% și 13% dintre femeile din această grupă de vârstă la nivel global, iar în România, estimările indică că cel puțin 1 din 10 femei fertile trăiește cu SOP — deseori fără să știe [1].
Cu toate acestea, SOP rămâne unul dintre sindroamele cel mai frecvent subdiagnosticate și, paradoxal, unul dintre cele mai frecvent diagnosticate incorect. Multe femei primesc diagnosticul abia după ani de simptome ignorate sau etichetate altfel: „cicluri neregulate de stres", „acnee hormonală fără importanță" sau „pur și simplu dificil de slăbit".
Scopul acestui articol este să explice clar ce este SOP, cum funcționează, de ce afectează atât de multe aspecte ale sănătății feminine — inclusiv fertilitatea — și ce soluții medicale integrate există astăzi pentru a-l gestiona eficient.
Ce este Sindromul Ovarelor Polichistice: definiție și criteriile de diagnostic
SOP este o afecțiune endocrino-metabolică complexă, caracterizată prin dereglarea axei hipotalamo-hipofizo-ovariene, cu consecințe hormonale, metabolice și reproductive.
Criteriile Rotterdam — standardul internațional de diagnostic
Diagnosticul de SOP este stabilit conform Criteriilor Rotterdam (2003), revizuite și validate de ghidurile internaționale actuale, prin prezența a cel puțin două din trei criterii [2]:
1. Oligo- sau anovulație — cicluri menstruale neregulate (mai rare de 8 cicluri/an), absente (amenoree) sau foarte frecvente, indicând tulburarea ovulației.
2. Hiperandrogenism clinic și/sau biochimic — semne clinice de exces androgenic (hirsutism, acnee, alopecie androgenică) și/sau valori crescute ale testosteronului total/liber sau altor androgeni în analize.
3. Morfologie ovariană polichistică la ecografie — prezența a ≥20 foliculi cu diametrul de 2–9 mm pe ovar și/sau volum ovarian >10 ml, în absența unui folicul dominant sau a unui corp galben
Important: este obligatorie excluderea altor diagnostice care pot mima SOP: hiperplazia congenitală de suprarenale (forma tardivă), hiperprolactinemia, disfuncțiile tiroidiene, tumorile secretante de androgeni și sindromul Cushing [3].
SOP nu este o boală — este un sindrom
Această distincție contează: SOP nu are o singură cauză și nu arată identic la toate femeile. Unele au cicluri neregulate și hirsutism, altele au infertilitate și rezistență la insulină, altele au aspect ecografic polichistic fără simptome semnificative. Prezentarea clinică este extrem de variabilă, ceea ce face ca diagnosticul să necesite evaluare medicală completă și individualizată.
Epidemiologie: cât de frecvent este SOP?
SOP este cea mai frecventă cauză de infertilitate anovulatorie și reprezintă aproximativ 75–80% din cazurile de infertilitate prin anovulație [4]. La nivel global:
Prevalența estimată: 8–13% din femeile de vârstă fertilă [1]
Până la 70% dintre cazuri rămân nediagnosticate în comunitate [5]
SOP este diagnosticat cel mai frecvent între 20 și 30 de ani, deși simptomele pot debuta de la pubertate
Riscul de SOP este influențat genetic — fiicele și surorile femeilor cu SOP au un risc semnificativ crescut [6]
Fiziopatologia SOP: ce se întâmplă în organism
Înțelegerea mecanismului SOP este esențială pentru a înțelege de ce el are atât de multe fețe și de ce tratamentul trebuie să fie întotdeauna individualizat.
1. Dereglarea axei LH/FSH
În SOP, raportul LH/FSH este frecvent crescut (≥2), ceea ce reflectă o anomalie în pulsatilitatea GnRH (hormonul eliberator de gonadotropine). Nivelul crescut de LH stimulează excesiv celulele tecale ovariene să producă androgeni, în timp ce FSH insuficient nu poate induce maturarea completă a foliculilor — rezultând anovulație și aspectul ecografic caracteristic de „colier de perle" [7].
2. Hiperandrogenismul ovarian
Excesul de androgeni (testosteron, androstendionă, DHEA-S) produse de ovar — și parțial de suprarenale — blochează maturarea foliculară, perturbă ovulația și generează manifestările clinice caracteristice: hirsutism, acnee, alopecie androgenă.
3. Rezistența la insulină și hiperinsulinismul compensator
Aproximativ 50–70% dintre femeile cu SOP prezintă rezistență la insulină, indiferent de greutatea corporală [8]. Hiperinsulinismul compensator amplifică producția ovariană de androgeni prin stimularea directă a celulelor tecale și scade sinteza hepatică a SHBG (globulina transportoare a hormonilor sexuali), crescând astfel fracțiunea liberă (activă) a testosteronului. Acest cerc vicios androgenic-insulinic este unul dintre pilonii centrali ai fiziopatologiei SOP.
4. Inflamația cronică de grad redus
Studiile au demonstrat că femeile cu SOP prezintă markeri inflamatori crescuți (CRP, IL-6, TNF-α), chiar și în absența obezității. Inflamația cronică de grad redus contribuie la rezistența la insulină, la disfuncția ovariană și la riscul cardiovascular crescut pe termen lung [9].
5. Disfuncția axei hipotalamo-hipofizo-suprarenale
La unele paciente cu SOP, suprarenalele contribuie semnificativ la excesul androgenic (DHEA-S crescut), indicând o componentă adrenală importantă care trebuie evaluată și adresată separat.
Simptomele SOP: cum se manifestă
SOP este un sindrom multifazial. Manifestările clinice pot varia de la o pacientă la alta, în funcție de fenotipul dominant. Simptomele se pot instala treptat, uneori de la primele cicluri menstruale (perimenarhă), alteori ulterior.
Tulburări menstruale
Oligomenoree — cicluri menstruale rare (interval >35 zile)
Amenoree — absența menstruației ≥3 luni consecutiv
Cicluri neregulate cu variabilitate semnificativă de la un ciclu la altul
Rar: sângerări disfuncționale (din cauza hiperplaziei endometriale în absența ovulației)
Menstruațiile neregulate sunt deseori primul semnal și sunt cauzate de anovulație sau oligovulație cronică — ovulul nu se eliberează la timp sau nu se eliberează deloc.
Semne de hiperandrogenism
Hirsutism — creșterea excesivă a pilozității în zone androgen-dependente (față, bărbie, buze, abdomen, coapse, sâni) — cel mai specific semn clinic de hiperandrogenism la femei; evaluat prin scorul Ferriman-Gallwey [10]
Acnee persistentă — mai ales la nivelul bărbiei, mandibulei și feței — rezistentă la tratamentele topice uzuale, cu componentă hormonală clară
Alopecie androgenică — subțierea difuză a firului de păr, în special la nivelul scalpului frontal și al vârfului capului
Seboreea — ten gras persistent
Simptome metabolice
Creștere în greutate dificil de controlat, cu distribuție adipoasă predominant abdominală (centrală)
Dificultăți în scăderea în greutate, chiar și în regim alimentar corect
Acantosis nigricans — hiperpigmentare catifelată la nivelul gâtului, axilelor sau inghinal, semn clasic de rezistență la insulină
Manifestări psihologice
Studiile arată că femeile cu SOP au rate semnificativ crescute de anxietate, depresie și tulburări ale imaginii corporale față de populația generală — consecință atât a dezechilibrelor hormonale, cât și a impactului simptomelor vizibile (hirsutism, acnee, greutate) asupra stimei de sine [11].
Aspectul ecografic
Ecografia transvaginală poate evidenția ovarele mărite în volum, cu multipli foliculi mici (2–9 mm diametru) distribuiți periferic în aspect caracteristic de „colier de perle" (≥20 foliculi pe ovar conform criteriilor actuale). Este important de subliniat că aspectul ecografic „polichistic" al ovarelor nu este suficient singur pentru diagnosticul de SOP — el trebuie corelat cu tabloul clinic și hormonal complet.
Impactul SOP asupra fertilității
SOP este cea mai frecventă cauză de infertilitate anovulatorie la femeia de vârstă fertilă [4]. Mecanismele prin care SOP afectează fertilitatea sunt multiple:
Anovulația cronică
Absența sau raritatea ovulației este principalul mecanism de infertilitate în SOP. Fără ovulație nu există ovul disponibil pentru fecundare, deci concepția spontană devine dificilă sau imposibilă.
Calitatea ovocitelor
Hiperandrogenismul și hiperinsulinismul afectează micromediul folicular, influențând negativ calitatea ovocitelor și rata de fertilizare, chiar și atunci când ovulația este indusă [12].
Calitatea endometrului
Lipsa progesteronului post-ovulator (din cauza anovulației) duce la expunerea cronică la estrogen necontraponderată, cu efecte negative asupra endometrului: hiperplazie, receptivitate alterată la implantare, risc crescut de avort precoce [13].
Riscuri în sarcina la pacientele cu SOP
Femeile cu SOP care obțin sarcina (spontan sau după inducția ovulației) au un risc crescut față de populația generală pentru:
Avort spontan precoce — datorat calității endometriale și excesului androgenic [14]
Diabet gestațional — pe fondul rezistenței la insulină preexistente [15]
Hipertensiune gestațională și preeclampsie [15]
Naștere prematură [16]
Macrosomie fetală (mai ales în context de diabet gestațional)
Aceste riscuri justifică monitorizarea atentă a sarcinii la pacientele cu SOP, de preferință de către un medic obstetrician familiarizat cu particularitățile acestui sindrom.
Complicațiile pe termen lung ale SOP
SOP nu este doar o problemă de ciclu menstrual sau de fertilitate. Dacă este lăsat netratat sau nesupravegheat, SOP poate genera complicații metabolice și oncologice semnificative pe termen lung:
Diabet zaharat de tip 2
Rezistența la insulină prezentă în SOP crește substanțial riscul de diabet zaharat de tip 2. Femeile cu SOP au un risc de 2–4 ori mai mare de a dezvolta DZ2 față de femeile fără SOP [17].
Sindromul metabolic
SOP se asociază frecvent cu sindromul metabolic (obezitate abdominală, dislipidemie, hipertensiune, hiperglicemie), cu implicații cardiovasculare importante pe termen lung [18].
Risc cardiovascular crescut
Hipertensiunea, dislipidemia, rezistența la insulină și inflamația cronică de fond din SOP contribuie la un profil de risc cardiovascular crescut, cu debut mai precoce față de femeile fără SOP [19].
Hiperplazia de endometru și riscul de cancer endometrial
Anovulația cronică înseamnă expunere prelungită la estrogen, fără contracararea progesteronului postovulator. Această stimulare estrogenică necontrolată crește riscul de hiperplazie endometrială și, pe termen lung, de cancer endometrial — cu un risc relativ de 2,7 ori mai mare față de populația generală [20].
Apneea obstructivă în somn
SOP se asociază cu un risc crescut de apnee obstructivă în somn (AOS), chiar și la femeile normoponderale — legătura fiind mediată de rezistența la insulină și hiperandrogenism [21].
Sănătatea mintală
Anxietatea, depresia și tulburările de anxietate sunt semnificativ mai frecvente la femeile cu SOP față de populație, atribuibile atât componentei hormonale, cât și impactului psihosocial al simptomelor vizibile [11].
Diagnosticul SOP: evaluarea completă, pas cu pas
Diagnosticul SOP necesită o abordare sistematică, care combină anamneza, examenul clinic, investigațiile hormonale și imagistica.
Anamneza și istoricul menstrual
Vârsta la prima menstruație (menarha) și caracterul ciclurilor de la debut
Frecvența, regularitatea și caracterul menstruațiilor actuale
Simptome de hiperandrogenism (pilozitate, acnee, căderea părului)
Modificări ponderale și distribuția grăsimii
Antecedente familiale de SOP, diabet, boli cardiovasculare, cancer endometrial
Dorință de concepție sau contracepție actuală
Examenul clinic
Indicele de masă corporală (IMC) și circumferința abdominală
Semne de hiperandrogenism: evaluarea pilozității (scorul Ferriman-Gallwey), acnee, alopecie
Semne de rezistență la insulină: acantosis nigricans
Tensiunea arterială
Examen ginecologic complet
Investigații hormonale și metabolice
Un profil hormonal complet este esențial pentru diagnosticul pozitiv și diferențial al SOP:
Hormoni de ax reproductiv:
FSH, LH (raport LH/FSH), estradiol — de preferat în zilele 2–5 ale ciclului
Prolactina — pentru excluderea hiperprolactinemiei
AMH (hormonul anti-Mülerian) — marker al rezervei ovariene și al numărului de foliculi antrali; frecvent crescut în SOP [22]
Androgeni:
Testosteron total și/sau liber
DHEA-S (de origine suprarenaliană)
Androstendionă
SHBG (globulina transportoare — frecvent scăzută în SOP, indicând fracțiune liberă crescută de testosteron)
Profil metabolic:
Glicemie a jeun și insulinemie a jeun (calcul HOMA-IR pentru evaluarea rezistenței la insulină)
Hemoglobina glicată (HbA1c)
Profil lipidic complet (colesterol total, LDL, HDL, trigliceride)
Hormoni tiroidieni:
TSH, FT4 — pentru excluderea hipotiroidismului, care poate mima SOP
Profil suprarenalian (când este indicat):
17-OH progesteron (matinal, în faza foliculară) — pentru excluderea hiperplaziei congenitale de suprarenale în formă tardivă
Cortizol urinar/seric — dacă există suspiciune de sindrom Cushing.
Ecografia transvaginală
Ecografia transvaginală cu aparat de înaltă rezoluție este investigația imagistică de referință în SOP:
Numărul foliculilor antrali pe ovar (≥20 foliculi de 2–9 mm = criteriu Rotterdam)
Volumul ovarian (>10 ml)
Grosimea endometrului (relevantă mai ales în anovulație cronică)
Excluderea chisturilor ovariene cu alte caracteristici.
Consultația ginecologică și ecografia sunt obligatorii și nu pot fi înlocuite de analize.
Alte investigații (selectiv)
Test de toleranță la glucoză (OGTT 75 g) — în prezența factorilor de risc pentru diabet gestațional sau DZ2
Ecografie mamară — în contextul evaluării complete a sănătății sânului
Densitometrie osoasă — la paciente cu amenoree prelungită.
Tratamentul SOP: abordarea integrată, pas cu pas
Nu există un tratament unic pentru SOP. Conduita terapeutică se personalizează în funcție de simptomele predominante, dorința de concepție, profilul metabolic și complicațiile asociate. Principalele obiective terapeutice sunt: regularizarea ciclului menstrual, reducerea hiperandrogenismului, ameliorarea rezistenței la insulină, protecția endometrului și, dacă este dorită, inducerea ovulației pentru concepție.
1. Modificarea stilului de viață — prima și cea mai importantă intervenție
Modificarea stilului de viață este prima linie de tratament în SOP la pacientele supraponderale sau obeze și are efecte demonstrate chiar și la normoponderale [23]:
Scăderea ponderală — chiar și o reducere de 5–10% din greutatea corporală poate restabili ovulația, reduce androgenemia și ameliora rezistența la insulină la femeile cu SOP supraponderale [23]
Alimentație echilibrată — dieta mediteraneană sau dieta cu index glicemic redus sunt asociate cu ameliorarea profilului hormonal și metabolic în SOP [24]
Activitate fizică regulată — minim 150 minute/săptămână de activitate aerobică moderată, cu efecte dovedite pe rezistența la insulină și pe profilul androgenic
Reducerea stresului cronic — stresul cronic activează axa hipotalamo-hipofizo-suprarenaliană și poate agrava dezechilibrele hormonale
2. Tratamentul medicamentos — individualizat în funcție de obiectiv
2a. Reglarea ciclului menstrual și protecția endometrului
Contraceptivele orale combinate (COC) rămân tratamentul de primă linie pentru reglarea ciclului menstrual, reducerea hiperandrogenismului și protecția endometrului la pacientele fără dorință imediată de concepție [25]. Prin suprimarea LH-ului și a producției ovariene de androgeni și prin creșterea SHBG, COC ameliorează atât neregularitățile menstruale, cât și hirsutismul și acneea.
Progestativele administrate ciclic (progesteron natural micronizat sau derivați sintetici) sunt o alternativă pentru inducerea menstruației și protecția endometrului, cu eficiență antiandrogenică mai redusă comparativ cu COC.
2b. Tratamentul rezistenței la insulină
Metforminul (biguanid) este tratamentul de referință pentru rezistența la insulină în SOP. Mecanismele sale includ reducerea producției hepatice de glucoză, ameliorarea sensibilității la insulină și, indirect, reducerea producției ovariene de androgeni [26]. Are și efect favorabil pe rata de ovulație spontană, pe reducerea riscului de avort precoce în sarcina din SOP și pe profilul metabolic pe termen lung. Nu se utilizează fără indicație medicală și monitorizare.
Inozitolul (myo-inozitol și D-chiro-inozitol) este un supliment cu dovezi clinice în creștere în SOP: ameliorează rezistența la insulină, reduce androgenemia și poate restabili ovulația la unele paciente [27]. Este considerat o opțiune sigură, cu profil bun de tolerabilitate.
2c. Tratamentul hiperandrogenismului
Spironolactona — antiandrogen cu efect bun pe hirsutism și acnee, utilizat în asociere cu contracepția (teratogen)
Acetat de ciproteron — antiandrogen potent, disponibil în anumite formulări de COC
Finasterida — inhibitor de 5α-reductază, utilizat selectiv în alopecia androgenică severă
2d. Inducerea ovulației (la pacientele cu dorință de concepție)
Inducerea ovulației în SOP trebuie realizată numai sub supraveghere medicală specializată, cu monitorizare ecografică obligatorie (foliculi seriali), din cauza riscului de hiperstimulare ovariană.
Letrozolul (inhibitor de aromatază) este recunoscut în ghidurile internaționale actuale (ESHRE/ASRM 2023) ca agent de primă linie pentru inducerea ovulației în SOP, cu rate de ovulație și de naștere vie superioare clomifenului [28].
Clomifen citrat — a fost mult timp standardul de aur, este mai ieftin și larg disponibil, dar recunoașterea ghidurilor s-a mutat spre letrozol.
Metformin + letrozol sau clomifen — combinația poate fi superioară monoterapiei la pacientele cu SOP și rezistență la insulină marcată [29].
FSH exogen (gonadotropine injectabile) — utilizate în cazul eșecului inducției orale, cu protocol step-up și monitorizare ecografică strictă.
Drilling ovarian laparoscopic — intervenție chirurgicală cu laser sau electrocauterizare la nivelul ovarelor, indicată la paciente cu SOP rezistent la inducția ovariană orală, cu rezultate în restabilirea ovulației la ~50–60% din cazuri [30].
3. Tratamentul complicațiilor metabolice
Monitorizarea și tratamentul dislipidemiei, hipertensiunii și prediabetului, în colaborare cu specialiști relevanți
Screening periodic pentru diabet gestațional în sarcina din SOP
Protecția endometrului pe termen lung prin menstruații induse cel puțin la 3–4 luni (progestativ sau COC), în special la pacientele cu anovulație cronică.
Monitorizarea pe termen lung a pacientelor cu SOP
SOP este o condiție cronică care necesită supraveghere periodică, nu doar tratament episodic. Recomandăm:
Consultație ginecologică + ecografie ovariană — ideal la 6 luni, cel puțin anual
Profil hormonal și metabolic — anual sau ori de câte ori simptomele se modifică
Screeningul pentru diabet (OGTT sau HbA1c) — la interval de 1–3 ani, în funcție de profilul de risc
Profil lipidic — anual
Monitorizarea endometrului — ecografic, mai ales în cazul anovulației de lungă durată
Suport psihologic — când este necesar, parte integrantă a managementului SOP.
Abordarea integrată la Clinica Doctor Allia Dmour din Iași
La Clinica Doctor Allia Dmour , SOP este abordat exact cum necesită complexitatea lui: integrat, cu ginecologia, endocrinologia și monitorizarea sarcinii, fără fragmentarea parcursului pacientei.
De ce abordarea integrată face diferența în SOP
SOP nu este o problemă strict ginecologică sau strict endocrinologică — este amândouă. O evaluare corectă a SOP necesită atât expertiza ginecologică (ecografie ovariană, evaluarea ciclului, a fertilității, a endometrului), cât și evaluarea endocrinologică completă (profil hormonal, metabolic, tiroidian, suprarenalian). Când aceste componente sunt evaluate și tratate de o echipă care comunică, rezultatele sunt semnificativ mai bune.
Ce oferim concret
Consultație ginecologică + ecografie ovariană: Examinare completă cu anamneză detaliată, examen clinic, ecografie transvaginală de înaltă rezoluție și stabilirea planului de investigații. Ecografia noastră folosește aparatură Voluson de înaltă performanță — relevantă mai ales pentru evaluarea precisă a morfologiei ovariene și a numărului foliculilor antrali.→ Ginecologie – Clinica Doctor Allia Dmour
Evaluare endocrinologică completă: Consultație endocrinologică cu evaluarea profilului hormonal reproductiv și metabolic (FSH, LH, estradiol, testosteron, DHEA-S, SHBG, AMH, prolactină, TSH, insulinemie, HOMA-IR, profil lipidic, glicemie), interpretarea corelată a rezultatelor și stabilirea conduitei terapeutice individualizate. Endocrinologia este esențială mai ales în SOP cu componentă metabolică importantă, cu rezistență la insulină sau cu dorință de concepție.→ Endocrinologie – Clinica Doctor Allia Dmour
Monitorizarea sarcinii la paciente cu SOP: Femeile cu SOP care obțin sarcina — spontan sau după inducția ovulației — beneficiază de monitorizare obstetricală atentă, în cunoștință de cauza riscurilor specifice (avort, diabet gestațional, preeclampsie). Monitorizarea sarcinii la Clinica Allia Ginecologie include ecografii seriate, investigații specifice trimestriale și consiliere adaptată fiecărui caz.→ Monitorizare sarcină – Clinica Doctor Allia Dmour
Inducerea ovulației sub monitorizare ecografică: Protocoalele de inducere a ovulației (letrozol, clomifen, metformin ± inductori) sunt administrate și monitorizate ecografic serial, cu ajustarea dozelor și evaluarea răspunsului folicular pentru maximizarea eficienței și minimizarea riscului de hiperstimulare.
Când să vii la consultație
Te adresezi unui specialist când:
Ai cicluri menstruale rare, neregulate sau absente de mai mult de 3–6 luni
Ai semne de hiperandrogenism: pilozitate excesivă în zone sensibile, acnee hormonală persistentă, căderea firului de păr
Încerci o sarcină de mai mult de 6–12 luni fără succes
Ai luat în greutate recent și ai dificultăți în a slăbi, mai ales cu distribuție abdominală
Ai antecedente familiale de SOP, diabet sau boli cardiovasculare precoce
Ai primit diagnosticul de SOP și nu ai un plan de monitorizare și tratament activ
Întrebări frecvente (FAQ)
SOP se vindecă?SOP nu are un tratament curativ definitiv — este o condiție cronică, dar foarte bine gestionabilă cu conduita corectă. Multe femei cu SOP trăiesc o viață normală, cu cicluri regulate, fertilitate păstrată și fără complicații metabolice, datorită unui management medical corect și activ.
Pot rămâne însărcinată cu SOP?Da. Majoritatea femeilor cu SOP pot obține o sarcină, fie spontan (mai ales după modificarea stilului de viață și echilibrarea hormonală), fie cu ajutorul inducției ovulației. Succesul depinde de vârstă, de durata tentativelor, de profilul hormonal și de complicațiile asociate. Este esențial să nu amânați consultația medicală dacă nu reușiți concepția în 6–12 luni.
Trebuie să slăbesc pentru ca tratamentul SOP să funcționeze?La pacientele supraponderale, pierderea în greutate este cel mai eficient tratament și poate restabili ovulația mai eficient decât medicamentele. Totuși, SOP apare și la femei normoponderale sau slabe — la acestea, abordarea este diferită și nu se pune accent pe slăbire, ci pe echilibrarea hormonală și metabolică.
SOP dispare la menopauză?Parțial — odată cu declinul funcției ovariene, anovulația și unele simptome hormonale se ameliorează sau dispar. Totuși, componenta metabolică a SOP (rezistența la insulină, riscul de diabet, riscul cardiovascular) persistă și după menopauză, motiv pentru care supravegherea medicală pe termen lung rămâne importantă.
Anticoncepționalele „tratează" SOP?COC reglează ciclul menstrual, reduc androgenemia și protejează endometrul — deci controlează simptomele. Dar nu „vindecă" SOP: la oprirea contracepției, dezechilibrele hormonale revin de obicei. Tocmai de aceea, COC nu este singurul tratament, ci parte dintr-o strategie mai amplă, individualizată.
Dieta poate îmbunătăți SOP?Da, semnificativ. Dieta mediteraneană și alimentele cu indice glicemic scăzut sunt asociate cu reducerea insulinemiei, a androgenemiei și cu ameliorarea funcției ovulatorii în SOP. Dieta nu înlocuiește tratamentul medical, dar potențează efectele acestuia considerabil.
Concluzie
Sindromul Ovarelor Polichistice (SOP) este o condiție complexă, cu implicații hormonale, metabolice, reproductive și psihologice — dar există soluții medicale cu rezultate foarte bune atunci când este diagnosticat corect și abordat integrat. Cheia nu este să suportați simptomele în tăcere, ci să le înțelegeți și să găsiți, alături de medicul dumneavoastră, un plan personalizat care să funcționeze pentru dumneavoastră.
🩺Aveți întrebări sau nevoie de îndrumare? Suntem aici pentru dumneavoastră!
📞 0747 619 919
📍Bd. Carol I nr. 48, Iași
Disclaimer medical
Informațiile din acest articol au caracter educativ general și nu constituie sfat medical individual. Diagnosticul și tratamentul SOP trebuie stabilite întotdeauna în urma consultației medicale, pe baza evaluării individuale a fiecărei paciente.
Referințe bibliografice
[1] March WA, Moore VM, Willson KJ, et al. The prevalence of polycystic ovary syndrome in a community sample assessed under contrasting diagnostic criteria. Hum Reprod. 2010;25(2):544-551.
[2] Rotterdam ESHRE/ASRM-Sponsored PCOS Consensus Workshop Group. Revised 2003 consensus on diagnostic criteria and long-term health risks related to polycystic ovary syndrome. Fertil Steril. 2004;81(1):19-25.
[3] Azziz R, Carmina E, Dewailly D, et al. Criteria for defining polycystic ovary syndrome as a predominantly hyperandrogenic syndrome. J Clin Endocrinol Metab. 2006;91(11):4237-4245.
[4] Balen AH, Morley LC, Misso M, et al. The management of anovulatory infertility in women with polycystic ovary syndrome. Hum Reprod Update. 2016;22(6):687-708.
[5] Boyle J, Teede HJ. Polycystic ovary syndrome — an update. Aust Fam Physician. 2012;41(10):752-756.
[6] Legro RS, Driscoll D, Strauss JF, et al. Evidence for a genetic basis for hyperandrogenemia in polycystic ovary syndrome. Proc Natl Acad Sci USA. 1998;95(25):14956-14960.
[7] McCartney CR, Marshall JC. Polycystic ovary syndrome. N Engl J Med. 2016;375(1):54-64.
[8] Dunaif A. Insulin resistance and the polycystic ovary syndrome: mechanism and implications for pathogenesis. Endocr Rev. 1997;18(6):774-800.
[9] Escobar-Morreale HF, Luque-Ramírez M, González F. Circulating inflammatory markers in polycystic ovary syndrome. Fertil Steril. 2011;95(3):1048-1058.
[10] Ferriman D, Gallwey JD. Clinical assessment of body hair growth in women. J Clin Endocrinol Metab. 1961;21:1440-1447.
[11] Dokras A, Clifton S, Futterweit W, Wild R. Increased prevalence of anxiety symptoms in women with polycystic ovary syndrome. Fertil Steril. 2012;97(1):225-230.
[12] Dumesic DA, Oberfield SE, Stener-Victorin E, et al. Scientific statement on the diagnostic criteria, epidemiology, pathophysiology, and molecular genetics of polycystic ovary syndrome. Endocr Rev. 2015;36(5):487-525.
[13] Palomba S, Falbo A, La Sala GB. Metformin and gonadotropins for ovulation induction in patients with polycystic ovary syndrome. Hum Reprod Update. 2014;20(1):100-119.
[14] Qin JZ, Pang LH, Li MJ, et al. Obstetric complications in women with polycystic ovary syndrome. Sci Rep. 2013;3:2762.
[15] Boomsma CM, Eijkemans MJ, Hughes EG, et al. A meta-analysis of pregnancy outcomes in women with polycystic ovary syndrome. Hum Reprod Update. 2006;12(6):673-683.
[16] Kjerulff LE, Sanchez-Ramos L, Duffy D. Pregnancy outcomes in women with polycystic ovary syndrome. Am J Obstet Gynecol. 2011;204(6):558.e1-6.
[17] Legro RS, Kunselman AR, Dodson WC, Dunaif A. Prevalence and predictors of risk for type 2 diabetes mellitus and impaired glucose tolerance in polycystic ovary syndrome. J Clin Endocrinol Metab. 1999;84(1):165-169.
[18] Apridonidze T, Essah PA, Iuorno MJ, Nestler JE. Prevalence and characteristics of the metabolic syndrome in women with polycystic ovary syndrome. J Clin Endocrinol Metab. 2005;90(4):1929-1935.
[19] Wild RA, Carmina E, Diamanti-Kandarakis E, et al. Assessment of cardiovascular risk and prevention of cardiovascular disease in women with the polycystic ovary syndrome. J Clin Endocrinol Metab. 2010;95(5):2038-2049.
[20] Barry JA, Azizia MM, Hardiman PJ. Risk of endometrial, ovarian and breast cancer in women with polycystic ovary syndrome. Hum Reprod Update. 2014;20(5):748-758.
[21] Vgontzas AN, Legro RS, Bixler EO, et al. Polycystic ovary syndrome is associated with obstructive sleep apnea and daytime sleepiness. J Clin Endocrinol Metab. 2001;86(2):517-520.
[22] Dewailly D, Andersen CY, Balen A, et al. The excess in polycystic follicles of women with PCOS is not due to increased serum AMH but to a defect in follicular selection. Hum Reprod. 2016;31(2):394-401.
[23] Teede HJ, Misso ML, Costello MF, et al. Recommendations from the international evidence-based guideline for the assessment and management of polycystic ovary syndrome. Hum Reprod. 2018;33(9):1602-1618.
[24] Barrea L, Arnone A, Annunziata G, et al. Adherence to the Mediterranean diet, dietary patterns and body composition in women with polycystic ovary syndrome. Nutrients. 2019;11(10):2278.
[25] Morotti E, Battaglia B, Persico N, et al. Ethinylestradiol/cyproterone acetate versus ethinylestradiol/drospirenone in the treatment of polycystic ovary syndrome. Gynecol Endocrinol. 2013;29(1):32-35.
[26] Tang T, Lord JM, Norman RJ, et al. Insulin-sensitising drugs (metformin, rosiglitazone, pioglitazone, D-chiro-inositol) for women with polycystic ovary syndrome, oligo amenorrhoea and subfertility. Cochrane Database Syst Rev. 2012;(5):CD003053.
[27] Unfer V, Nestler JE, Kamenov ZA, et al. Effects of inositol(s) in women with PCOS: a systematic review of randomized controlled trials. Int J Endocrinol. 2016;2016:1849162.
[28] Legro RS, Brzyski RG, Diamond MP, et al. Letrozole versus clomiphene for infertility in the polycystic ovary syndrome. N Engl J Med. 2014;371(2):119-129.
[29] Palomba S, Orio F Jr, Falbo A, et al. Clomiphene citrate versus metformin as first-line approach for the treatment of anovulation in infertile patients with polycystic ovary syndrome. J Clin Endocrinol Metab. 2007;92(9):3498-3503.
[30] Farquhar C, Brown J, Marjoribanks J. Laparoscopic drilling by diathermy or laser for ovulation induction in anovulatory polycystic ovary syndrome. Cochrane Database Syst Rev. 2012;(6):CD001122.



Comments